 Почти все отзывы об изделиях медицинского назначения добровольно выдаются фирмами, а не по требованию FDA. wavebreakmedia / shutterstock.com
Почти все отзывы об изделиях медицинского назначения добровольно выдаются фирмами, а не по требованию FDA. wavebreakmedia / shutterstock.com
Из издания Валсартан кровяное давление наркотиков загрязнение которые подвергли тысячи пациентов воздействию канцерогенных примесей, массивный отзыв кардиостимулятора Предпринятые для исправления опасной ошибки в программном обеспечении в полумиллионе сердечных устройств, проблемы с качеством медицинской продукции всегда и очень опасны.
По факту, медицинский продукт отзывает - в особенности тяжелые, опасные для жизни фармацевтический препарат и медицинский прибор напоминает - есть неуклонно растет в течение последнего десятилетия.
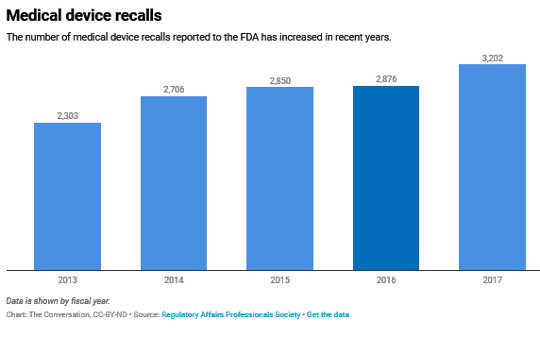
Неудивительно, что отзыв лекарственных средств является повсеместно негативным явлением. Фирмы стремятся их избегать, клиенты их презирают, а федеральные регуляторы вынуждены их контролировать. Они связаны с миллионы долларов нежелательных корпоративных расходов и снижение цен на акции, наряду с существенным и дорогостоящим надзорным контролем каждый год.
Я провел более десяти лет в качестве менеджера по производству в компаниях по производству медицинского оборудования Fortune 500, делая множество отзывов и рекомендаций - некоторые хорошие решения, некоторые менее - и последние несколько лет как академический исследователь, стремящийся только отозвать исследование, Мои коллеги и я внимательно изучили причины дефектов, которые приводят к отзыву, а также предвзятости, которые существуют в решениях менеджеров по отзыву.
Чрезмерная стоимость конкуренции
На капиталистических рынках конкуренция рассматривается как сила добра. Конкуренция может снизить затраты, расширить доступ и, возможно, улучшить качество. Эти преимущества, связанные с конкуренцией, объясняют постоянный призыв к расширению доступа к непатентованным лекарствам.
Хотя это редко обсуждается в многолюдных дебатах о расходах на здравоохранение, может быть обратная сторона бесконечного призыва к более дешевым непатентованным лекарствам и более доступному уходу.
Исследование проведено с моими коллегами Рачна Шах из Университета Миннесоты и Кейтлин Ваук из Университета Нотр-Дам показывает, что интенсивная конкуренция с использованием дженериков приводит к увеличению количества крайне опасных отзывов о производстве наркотиков.
Наше исследованиеВ мае 2018, опубликованный в мае, показывает, что конкуренция с генерическими лекарственными средствами заставляет фирмы сокращать свои позиции в области контроля качества производства, стремясь оставаться прибыльными, что ведет к увеличению количества опасных для жизни дефектов лекарств, требующих отзыва.
Одним из многих примеров такого типа проблем является недавнее Ранбакси аторвастатин отзыв, Провалы в системе контроля качества производства привели к загрязнению от несанкционированного сырья. Производитель дженериков согласился Государственный штраф в размере 500 миллионов долларов США.
 Количество медицинских изделий выросло за последнее десятилетие. Ацуши Хирао / shutterstock.com
Количество медицинских изделий выросло за последнее десятилетие. Ацуши Хирао / shutterstock.com
Знакомые инспекторы FDA
Одним из способов помочь смягчить такие неблагоприятные побочные эффекты конкуренции являются нормативные акты Управления по контролю за продуктами и лекарствами США и методы контроля качества.
Основным инструментом, используемым FDA для улучшения качества продукции, являются инспекции растений. Инспекторы FDA посещают заводы с двухлетним циклом вращения. Эти оценки результатов проверки могут быть ранним предупреждением о будущих отзывах с завода - если инспектор FDA точно фиксирует соответствующие риски.
В исследовании 2017 с шахом и Энно Симсен из Университета Висконсин-МэдисонМы обнаружили, что рейтинги результатов FDA могут быть использованы для прогнозирования будущих отзывов продуктов, произведенных на этом заводе. Однако это верно только тогда, когда инспектор никогда не посещал завод раньше.
Чрезмерное знакомство между инспекторами FDA и руководством завода ослабляет точность оценок даже после одной повторной проверки. Инспекторы становятся удовлетворенными, поскольку они становятся более знакомыми с заводом и людьми, которые там работают.
Мы обнаружили, что чередование новых инспекторов для каждой инспекции завода FDA значительно повысит ценность этих инспекций и будет стоить FDA менее 1 миллионов долларов в год. Небольшая цена за безопасность медицинского устройства.
Управленческие уклоны
В то время как регулирующий надзор может помочь уменьшить количество бракованной продукции, требующей отзыва, еще одним важным аспектом явления отзыва являются менеджеры, которые решили отозвать продукт.
Интересно, что почти все отзывы на медицинские изделия производятся фирмами добровольно, а не по требованию FDA. Добровольный характер этих отзывов дает руководителям высокий уровень свободы действий при принятии решения об отзыве.
Я работал с Шахом и Карен Донохью в Университете Миннесоты в изучать управленческие уклоны при отзыве решений, принятых реальными руководителями отрасли.
Один из них связан с врачами, которые покупают медицинские приборы от имени пациентов. Если менеджеры знают, что их клиенты-врачи, скорее всего, обнаружат дефект в устройстве перед использованием продукта на пациенте, то менеджеры на удивление будут реже вспоминать. Они неосознанно доверяют врачу отсеивать обнаруживаемые дефекты, устраняя необходимость отзыва.
Этот уклон был неизвестен менеджерам, которые участвовали в этом исследовании. Фирмы, с которыми мы работали, использовали эти результаты для обучения лиц, принимающих решения, осознанию этого нежелательного смещения.
В том же исследовании мы провели тест поведенческого познания на менеджеров, прежде чем они приняли решение отозвать. Этот тест из трех вопросов измеряет, принимает ли человек решения на основе интуиции или рефлексии.
Этот тест очень объяснил, как менеджер принял решение об отзыве. Рефлексивные менеджеры вспоминают гораздо реже, так как они могут стремиться к «параличу анализа», ища чрезмерные объемы данных, прежде чем захотеть вспомнить. Это может объяснить, почему в ситуациях, когда рефлексивные менеджеры принимают решения об отзыве, фирмы, по-видимому, задерживают отзыв, даже если это повышает риск причинения вреда клиентам.
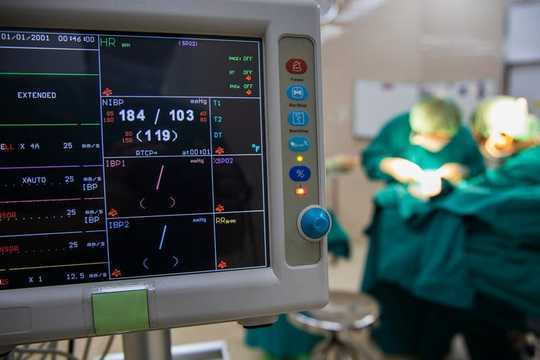 Врачи иногда обнаруживают дефект устройства на раннем этапе, еще до того, как оно использовалось у пациента. Питер Поррини / shutterstock.com
Врачи иногда обнаруживают дефект устройства на раннем этапе, еще до того, как оно использовалось у пациента. Питер Поррини / shutterstock.com
Другие причины
Несколько разных соавторов и я проводим другие захватывающие исследования, направленные на то, чтобы продолжить анализ этой важной проблемы, особенно с точки зрения управленческих ошибок.
Например, в одном рабочем документе говорится, что фирмы, выпускающие медицинские товары, с советами директоров, в состав которых входит хотя бы одна женщина, принимают решения об отзыве намного эффективнее и быстрее, чем фирмы с советами, состоящими исключительно из мужчин.
В другом рабочем документе говорится, что новые руководители в компаниях, производящих потребительские товары, похоже, козлы отпущения от предыдущего руководителя. Новые генеральные директора, как правило, объявляют о нескольких отзывах в начале своего срока полномочий, когда предыдущий генеральный директор, вероятно, будет обвинен в проблемах с качеством продукции.
Поскольку отзыв продукции широко распространен и часто связан с вредом для потребителя, я искренне надеюсь, что тщательные исследования продолжают разгадывать эту сложную загадку, пытаясь помочь фирмам, регуляторам и потребителям.![]()
Об авторе
Джордж Болл, доцент кафедры операций и технологий принятия решений, Школа бизнеса Келли, Университет Индианы
Эта статья переиздана из Беседа под лицензией Creative Commons. Прочтите оригинал статьи.
Книги по этой теме
at Внутренний рынок самовыражения и Amazon
























